

比利时的一项新研究发表在《Science》杂志上,研究团队探讨了基因开关如何通过控制基因活动来定义不同物种的脑细胞类型。
研究人员使用了人类、小鼠和鸡的大脑数据来训练深度学习模型,并发现,尽管某些细胞类型在经过数百万年的进化后在鸟类和哺乳动物之间得到了高度保守,但其它细胞类型的进化方式却存在显著差异。
这些发现不仅为大脑进化提供了崭新的视角,同时也为研究基因调控如何在不同细胞类型之间、跨物种或者在不同疾病状态下发挥作用提供了有力工具。
该研究以「Enhancer-driven cell type comparison reveals similarities between the mammalian and bird pallium」为题,定于2025年2月14日在《Science》上发布。
我们的脑和整个身体由多种不同类型的细胞构成。尽管这些细胞共享相同的 DNA,它们却拥有各自独特的形状和功能。
每种细胞类型的差异是一个复杂的难题,研究人员几十年来一直在通过分析充当基因开关的短 DNA 序列来解答这一谜团。这些序列控制着哪些基因被激活或抑制。
这些开关的精细调节确保了每种脑细胞能够利用基因组中的正确遗传指令,发挥其特定功能。科学界将这些基因开关的独特模式称为调控代码。
VIB Center for AI & Computational Biology 与 VIB-KU Leuven Center for Brain & Disease Research 的Stein Aerts教授及其团队对这种调控代码的基本原理进行了研究,以分析其在癌症或脑部疾病等疾病中的影响。
他们开发了新的深度学习方法,以帮助理解从成千上万个单一细胞中收集的大量基因调控信息。
Aerts表示:“通过使用 DNA 序列代码的深度学习模型,我们能够显著识别不同细胞类型的调控机制。接下来,我们希望探讨这种调控代码是否也能揭示这些细胞类型在物种间的保守性。”
大脑是一个高度相关的研究领域。尽管哺乳动物与鸟类的大脑有着共同的发育路线,但它们的神经解剖结构却存在显著差异。Aerts团队已将深度学习模型应用于评估这些差异与相似性是否反映在共同或不同的调控代码中。
研究进化的工具
Nikolai Hecker及Niklas Kempynck分别是Aerts实验室的博士后和博士生,他们开发并实施了机器学习模型,以描述和比较人类、小鼠和鸡脑中不同类型的细胞组织,涵盖约3.2亿年的进化历程。
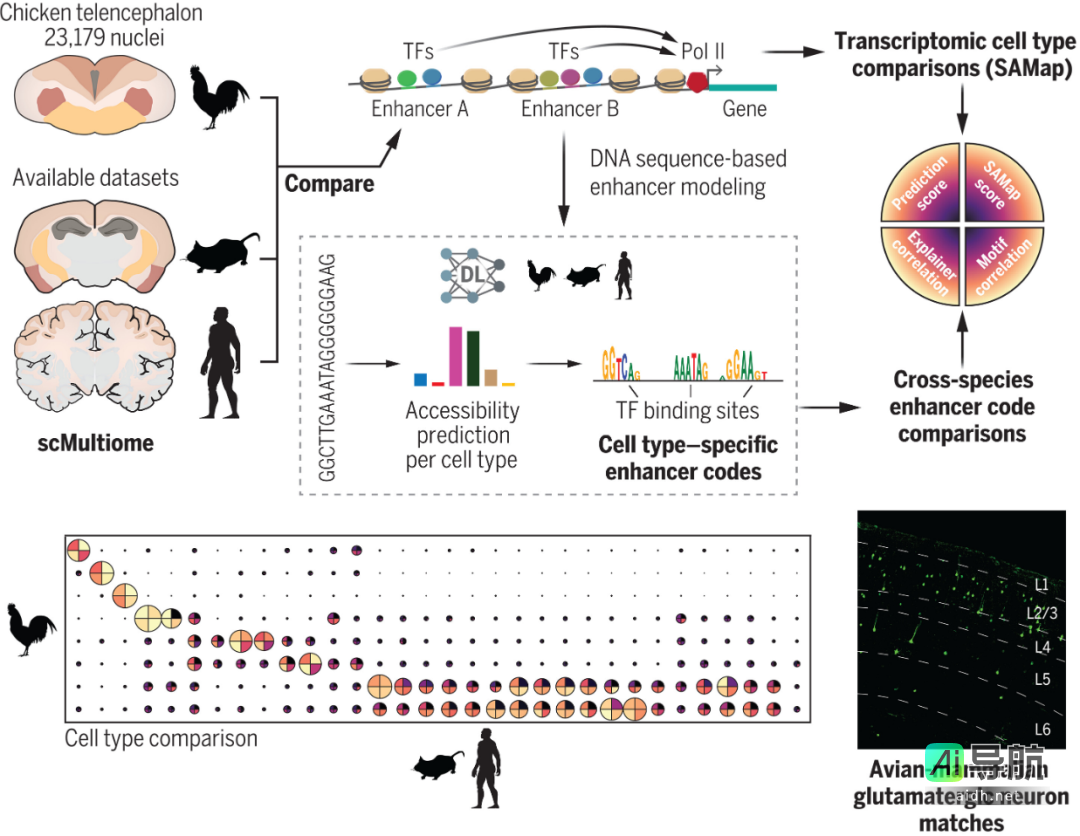
图示:鸟类与哺乳动物端脑调控代码之间的对应关系暗示了祖先的保守性。(来源:论文)
然而,在进行真正的比较之前,他们首先需要更好地了解鸡脑中的细胞类型组成。为了表征和比较哺乳动物与鸟类大脑皮层中的脑细胞类型增强子代码,该团队生成了鸡端脑的单细胞多组学(scMultiome)和空间解析转录组学数据。
作为比对物种间细胞类型相似性的基准,他们比较了人类、小鼠与鸡端脑细胞类型的转录组。随后,他们利用染色质可及性变异作为工具,识别潜在的基因组增强子区域并评估其细胞类型特异性。
接下来,研究人员在这些区域上训练了基于序列的深度学习模型,从而推断人类、小鼠与鸡端脑细胞类型特异性的增强子代码。
Hecker解释道:“我们的研究演示了如何运用深度学习根据其调控代码表征和比较不同细胞类型。我们可以利用这些代码比较不同物种的基因组,确定哪些调控代码在进化过程中得以保留,并深入理解细胞类型的进化机制。”
鸡端脑中的兴奋性神经元显著聚集于皮质神经解剖区域,包括中皮质、内皮质、超皮质及巢皮质。根据转录组与增强子代码的比较,非神经元与γ-氨基丁酸介导(GABAergic)细胞类型在鸟类与哺乳动物中表现出高度相似性,这在这些细胞类型的保守转录因子组合中得以体现。
相较之下,哺乳动物与鸟类大脑皮层的兴奋性神经元的增强子代码则表现出更高的分化程度。这些匹配结果仅部分符合现有的基于发育路径与脑回路的脊椎动物大脑皮层细胞类型同源进化模型。
之前的研究中,Aerts 团队已证实,哺乳动物与斑马鱼之间保留了黑色素瘤(皮肤癌)细胞状态的调控代码,并发现了黑色素瘤患者基因组中的变异。
本研究中提出的脑细胞类型模型为研究基因组变异的影响以及其与心理或认知特征和障碍的关系提供了有益的工具。
Aerts 表示:“最终,学习基因组调控代码的模型有潜力筛选基因组,并研究任何物种中特定细胞类型或细胞状态的存在。这将成为研究和深入了解疾病的有力工具。”
Aerts 团队已在两个方面应用其模型。他说:“我们与动物园科学以及野生动物救助中心的合作,使我们能够将我们的进化模型扩展到更多动物的大脑,包括不同类型的鱼、鹿、刺猬和水豚。同时,我们也在探讨这些人工智能模型如何帮助揭示与帕金森病相关的遗传变异。”
论文链接:[https://www.science.org/doi/10.1126/science.adp3957](https://www.science.org/doi/10.1126/science.adp3957)
相关报道:[https://phys.org/news/2025-02-deep-view-million-years-brain.html](https://phys.org/news/2025-02-deep-view-million-years-brain.html)
© 版权声明
文章版权归作者所有,未经允许请勿转载。
相关AI热点

暂无评论...






